一、新一代高选择性BTK抑制剂康可期®纳入2023版国家医保目录
国家医保局正式公布《国家基本医疗保险、工伤保险和生育保险药品目录(2023年版)》,阿斯利康新一代高选择性BTK抑制剂康可期®(通用名:阿可替尼胶囊,以下简称”阿可替尼”)成功准入医保目录,本品单药适用于既往至少接受过一种治疗的成人套细胞淋巴瘤(MCL)患者,极大提升该创新药物的可及性与可负担性,助力更多的中国MCL患者实现高质量长生存。
药物信息
药物名称:Acalabrutinib
适应症:成人套细胞淋巴瘤(MCL)
研发公司:阿斯利康
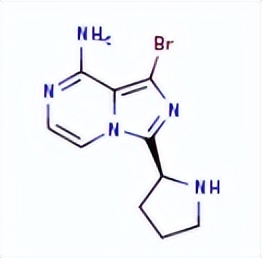
API结构
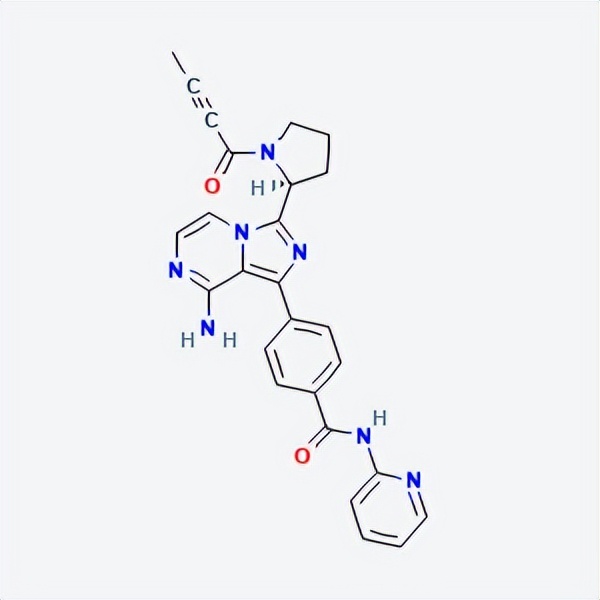
CAS:1420477-60-6
Acalabrutinib结构中韶远能够提供的小分子砌块
SY007445
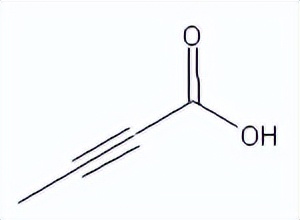
SY255575
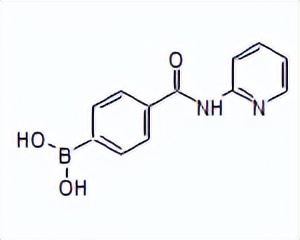
2097168-73-3
二、康哲药业:4款产品新纳入或继续纳入国家医保目录
康哲药业欣然宣布,根据中国国家医疗保障局及国家人力资源和社会保障部发布的通知,创新药地西泮鼻喷雾剂(维图可)及替瑞奇珠单抗注射液(益路取)、罕见病用药丁苯那嗪片新纳入中国《国家基本医疗保险、工伤保险和生育保险药品目录(2023年)》(”国家医保目录”)乙类范围,注射用重组人脑利钠肽(新活素)继续纳入国家医保目录乙类范围,并将自2024年1月1日起正式实施。此外,2023年3月获批的创新药甲氨蝶呤注射液-银屑病适应症(美泰彤)已纳入国家医保目录甲类范围。
其中:丁苯那嗪片
2023年5月,丁苯那嗪片于中国获批上市,用于治疗亨廷顿舞蹈症。丁苯那嗪片作为亨廷顿舞蹈症一线用药,有望为罕见病患者提供更多可及且可负担的用药选择。
康哲药业于2019年8月从Sun Pharmaceutical Industries Ltd.处获得丁苯那嗪片的独家许可权利。
药物信息
药物名称:Tetrabenazine
适应症:亨廷顿舞蹈症
研发公司:康哲药业
API结构
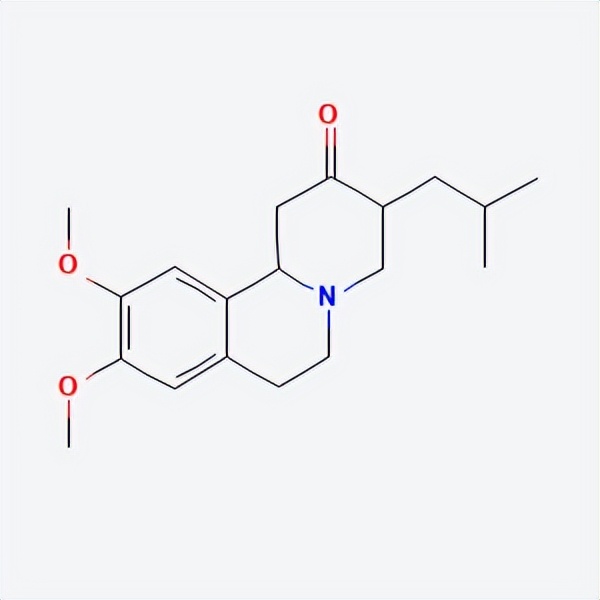
CAS:58-46-8
Tetrabenazine结构中韶远能够提供的小分子砌块
SY009731
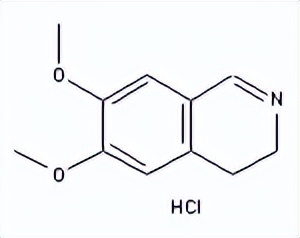
SY127415
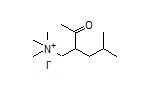
三、三代EGFR-TKI肺癌靶向药泰瑞沙®术后辅助治疗适应症纳入2023年版国家医保目录,助力早中期肺癌患者实现长生存
国家医保局公布了《国家基本医疗保险、工伤保险和生育保险药品目录(2023年)》,阿斯利康肺癌三代EGFR-TKI靶向药泰瑞沙®(通用名:甲磺酸奥希替尼片,以下简称”奥希替尼”)术后辅助治疗适应症成功准入医保目录,适用于IB-IIIA期存在表皮生长因子受体 (EGFR) 外显子19缺失或外显子21 (L858R) 置换突变的非小细胞肺癌 (NSCLC) 患者的治疗,患者须既往接受过手术切除治疗,并由医生决定接受或不接受辅助化疗。
药物信息
药物名称:Osimertinib mesylate
适应症:肺癌
研发公司:阿斯利康
API结构
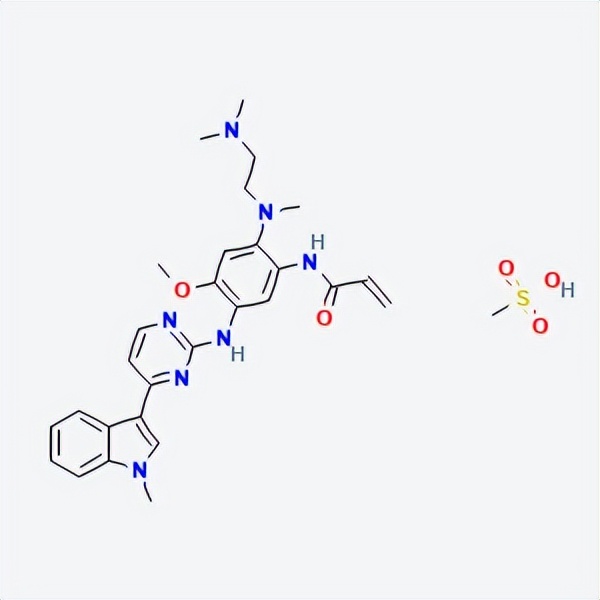
CAS:1421373-66-1
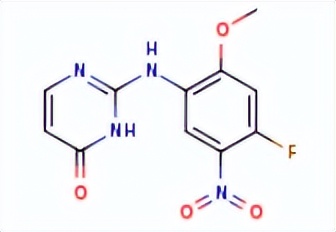
Osimertinib mesylate结构中韶远能够提供的小分子砌块
SY015321
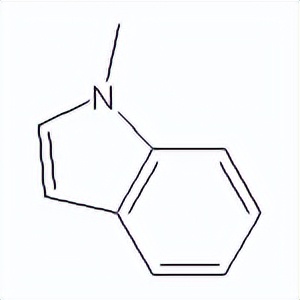
SY010366

2093274-72-5
四、Menarini Group在 2023 年圣安东尼奥乳腺癌研讨会上公布初步安全性和有效性数据
国际领先的制药和诊断公司 Menarini Group(简称”Menarini”)和 Menarini Group 旗下专注于为癌症患者带来变革性肿瘤治疗的全资子公司 Stemline Therapeutics, Inc.(简称”Stemline”)公布了 1b/2 期 ELEVATE 和 ELECTRA 评估 ORSERDU® (elacestrant) 联合治疗的临床研究结果。ELEVATE 和 ELECTRA 的研究旨在克服不同的耐药机制,并通过联合治疗方案提高疗效。数据已在 2023 年 12 月 5 日至 9 日举行的 2023 年圣安东尼奥乳腺癌研讨会 (SABCS) 上发布。
ELEVATE 研究项目正在评估 elacestrant 与 PI3K/AKT/mTOR 通路抑制剂(everolimus 和 alpelisib)以及细胞周期通路抑制剂(palbociclib、ribociclib 和 abemaciclib)的联合治疗。SABCS 2023 会议上公布了该研究 1b 期 Cohort 1 的所有联合治疗数据,研究结果显示这些疗法的安全性可以预测,且与此前研究保持一致。目前该研究正在对其他小组进行药物代谢动力学 (PK) 评估,并确定每种联合疗法的 2 期推荐剂量 (RP2D)。
药物信息
药物名称:Fenhexamid(Elevate)
适应症:乳腺癌
研发公司:Menarini Group
API结构
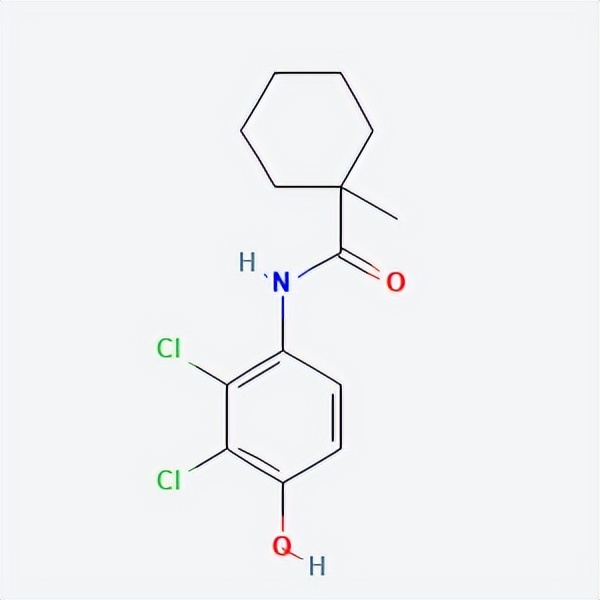
CAS:126833-17-8
Fenhexamid结构中韶远能够提供的小分子砌块
SY035149
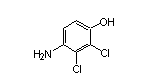
SY241587
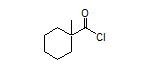
SY004269
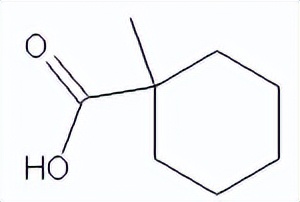
五、华领医药宣布多格列艾汀纳入国家医保药品目录
华领医药(”公司”,香港联交所股份代号:2552.HK)今日宣布,公司自主研发的糖尿病全球首创新药葡萄糖激酶激活剂(GKA)多格列艾汀(商品名:华堂宁®)成功纳入国家医疗保障局(”国家医保局”)发布的《国家基本医疗保险、工伤保险和生育保险药品目录》(”国家医保药品目录”)。多格列艾汀是华领医药首次参加医保谈判的首款商业化产品。此次顺利进入医保,标志着华领医药在商业化道路上的又一次重大突破。
多格列艾汀是华领医药根据”修复传感,重塑稳态,从源头上治疗糖尿病”的原创科学概念,自主研发的一款全球首创、全新机制、异位变构调节的GKA药物。多格列艾汀以人体血糖传感器葡萄糖激酶(GK)为靶点,作用于胰岛、肠道、肝脏等葡萄糖储存与输出器官,改善2型糖尿病患者受损的GK功能,进而改善β细胞功能,降低胰岛素抵抗。故而,具有重塑血糖平衡生理调节的作用机制,有望从源头上控制2型糖尿病的进展和并发症的发生。临床研究显示,部分患者接受多格列艾汀治疗后,停药后也能实现良好的血糖控制,有望实现糖尿病缓解。
药物信息
药物名称:Dorzagliatin
适应症:糖尿病
研发公司:华领医药
API结构
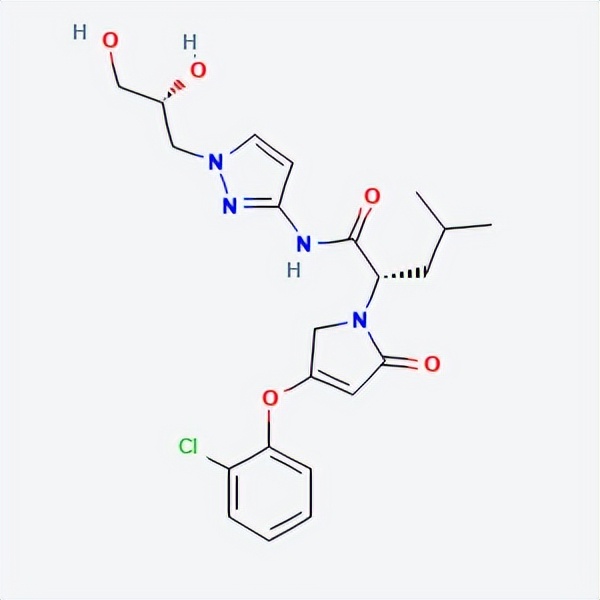
CAS:1191995-00-2
Dorzagliatin结构中韶远能够提供的小分子砌块
1174231-07-2
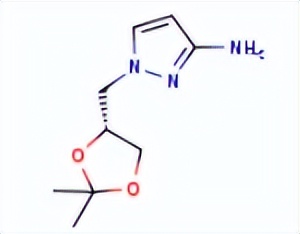
1191997-64-4
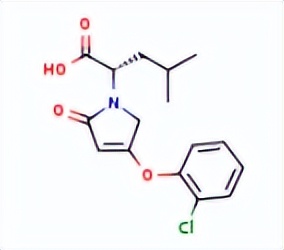
六、和誉医药创新CSF-1R抑制剂Pimicotinib(ABSK021)喜获FDA快速通道认定
和誉医药(港交所代码:02256)近日宣布,其创新CSF-1R抑制剂Pimicotinib(ABSK021)获美国食品药品监督管理局(“FDA”)授予快速通道认定(Fast Track Designation)用于治疗不可手术的腱鞘巨细胞瘤(“TGCT”)。此前,Pimicotinib于今年1月获得FDA授予的突破性疗法认定(Breakthrough Therapy Designation)。快速通道认定及突破性疗法认定将加速Pimicotinib在全球上市的步伐。
快速通道是FDA旨在促进药物开发和加快审查,以治疗严重疾病和满足未获满足的医疗需求的政策,其目的是为了更早地为患者提供重要的新药。除此之外,获得快速通道认定后可以帮助企业与FDA保持更为高频的沟通,并且药物将获得FDA的加速批准和优先审查。
药物信息
药物名称:Pimicotinib
适应症:腱鞘巨细胞瘤
研发公司:和誉医药
API结构
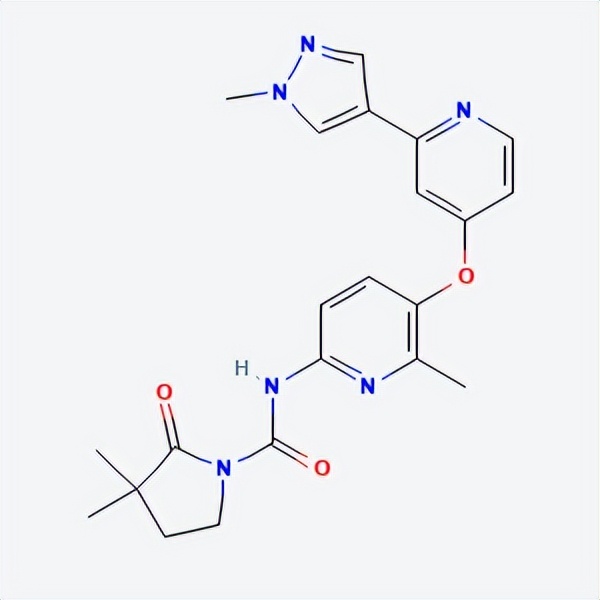
CAS:2253123-16-7
Pimicotinib结构中韶远能够提供的小分子砌块
SY067839
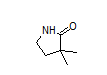
1628184-09-7
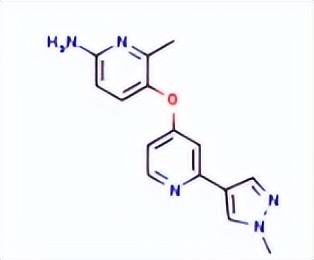
SY003667
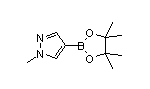
1628184-14-4
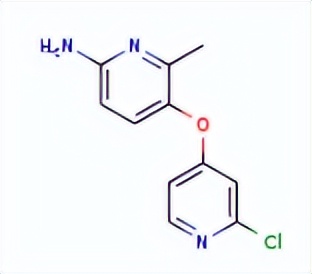
素材来源:药渡、Pubchem,若有侵权望联系删除!
