Primer probe combination and kit for detecting bovine respiratory diseases and application of primer probe combination and kit
A primer set and probe set technology, applied in the field of bovine respiratory virus detection, can solve the problems of time-consuming virus isolation and identification, low sensitivity, unfavorable diagnosis, etc., and achieve a wide range of sample application, good repeatability, and no potential biological safety hazard. Effects of ingredients
- Summary
- Abstract
- Description
- Claims
- Application Information
AI Technical Summary
Problems solved by technology
Method used
Image
Examples
Example Embodiment
[0066]实施例1引物与探针组的设计与筛选
[0067]引物的性能决定了试剂盒检测效果的优劣。本实施例针对检测指标牛传染性鼻气管炎病毒、牛病毒性腹泻病毒和牛支原体筛选了多组引物 / 探针组合,最终筛选到一组最优的引物 / 探针组合。本实施例旨在说明引物 / 探针组合的设计及筛选过程。
[0068]引物和探针的设计:下载GenBank上已登录的具有高度特异性的牛传染性鼻气管炎病毒的gB基因(序列号:MF287966.1)、牛病毒性腹泻病毒的5’-UTR基因(序列号:AF091605.1)和牛支原体的P48基因(序列号:KX772800.1),利用Primer Express5.0以及Oligo6.0设计软件,设计出扩增上述基因片段的特异性引物和荧光探针,并将设计得到的引物和探针进行BLAST验证,以保证引物的高特异性,经过验证,设计出如表1所示的9组引物和3组探针。
[0069]引物筛选:以牛传染性鼻气管炎病毒、牛病毒性腹泻病毒和牛支原体等病原提取的核酸的混合物的10倍梯度稀释的稀释物为模板,对所设计得到的牛传染性鼻气管炎病毒、牛病毒性腹泻病毒和牛支原体的3组引物分别进行单重荧光PCR反应,筛选出最佳的引物探针组合。单重荧光PCR的初始反应体系为:TaqDNA聚合酶(5U / μL)0.4μL,逆转录酶(5U / μL)0.4μL,2×PCR Buffer10μL,上下游引物(10μM)各0.4μL,探针(10μM)0.2μL,无核酶水6.2μL,模板2μL。反应程序:逆转录42℃5min;预变性94℃30s;变性94℃5s,退火60℃30s,40个循环。由表2可以看出,根据敏感性和扩增效率最终筛选出牛传染性鼻气管炎病毒、牛病毒性腹泻病毒和牛支原体的最佳引物组分别为:IBRV-F1(SEQ ID NO.1)、IBRV-R1(SEQ IDNO.2),BVDV-F1(SEQ ID NO.8)、BVDV-R1(SEQ ID NO.9),Mb-F2(SEQ ID NO.17)、Mb-R2(SEQID NO.18),即将上述三组引物作为本发明后续多重PCR反应的引物组。
[0070]表1引物和探针序列
[0071]
[0072]
[0073]表2引物筛选结果
[0074]
[0075]
[0076]注:0代表无Ct值。
Example Embodiment
[0077]实施例2阳性参考品制备
[0078]分别以牛传染性鼻气管炎病毒的cDNA、牛病毒性腹泻病毒和牛支原体的DNA为模板,使用实施例1筛选出的最佳引物组进行普通PCR扩增,电泳后分别获得117bp、105bp和132bp的目的片段。PCR产物使用琼脂糖凝胶DNA回收试剂盒(天根生化科技有限公司)回收并纯化,将纯化后的DNA片段克隆至pMD 19-T Vector(Takara),继而转化到DH5α(上海唯地生物技术有限公司),选取阳性克隆进行测序验证,验证合格后进一步扩增培养。分别将阳性菌液使用质粒小量提取试剂盒(天根生化科技有限公司)提取重组质粒。使用核酸蛋白测定仪测定其蛋白浓度,并根据公式[6.02×1023(拷贝 / moL)]×[浓度(g / μL)] / [MW(g / moL)]=拷贝数(copies / μL)计算出拷贝数,将三种重组质粒的浓度调整至1×106拷贝 / μL,然后将三种重组质粒按1:1:1进行混合即为阳性参考品。
Example Embodiment
[0079]实施例3三重荧光PCR检测方法建立并优化
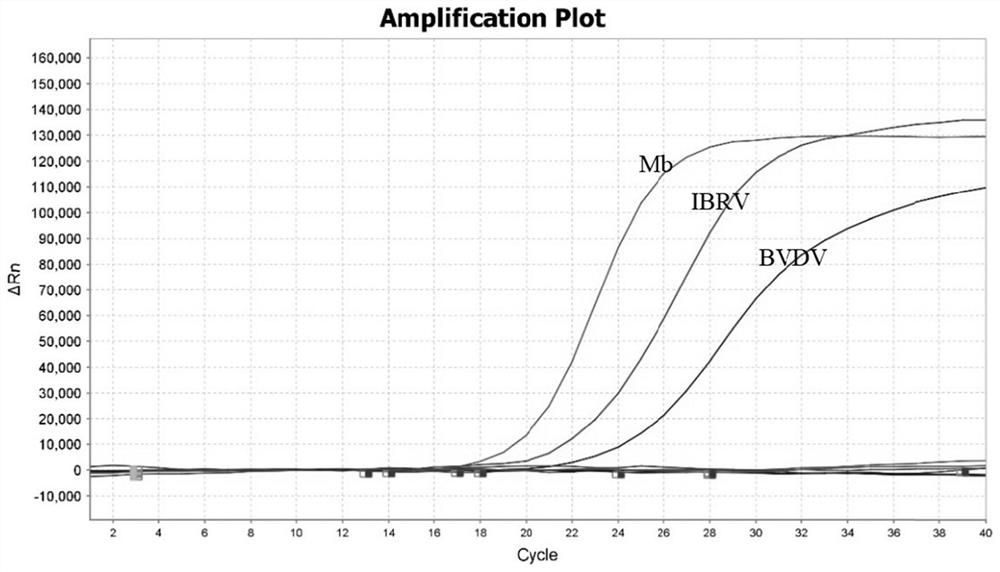
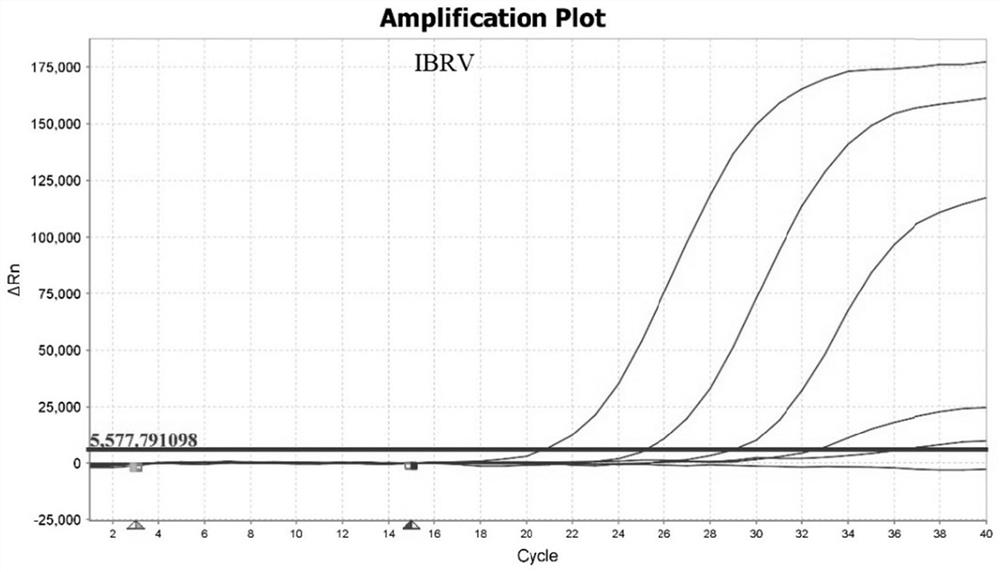
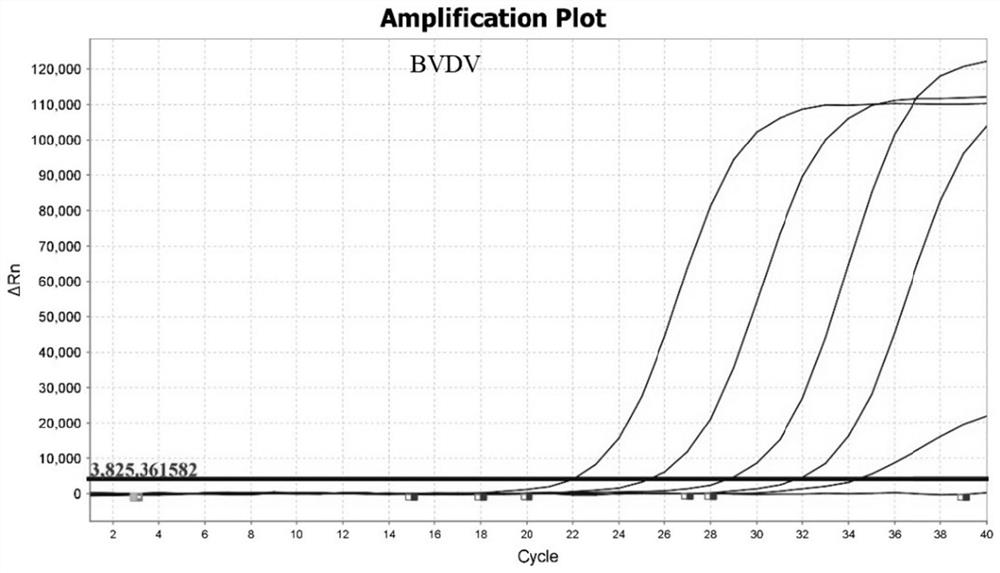
[0080]以3倍稀释的阳性参考品(由实施例2制得)为模板,分别进行牛传染性鼻气管炎病毒、牛病毒性腹泻病毒和牛支原体单重荧光PCR引物(上下引物浓度为1:1)和探针浓度梯度试验,根据扩增效率和敏感性分别确定牛传染性鼻气管炎病毒、牛病毒性腹泻病毒和牛支原体引物 / 探针浓度范围(得到引物终浓度范围为0.2~0.6μM,探针终浓度范围为0.1~0.3μM);然后根据确定的引物浓度范围选择牛传染性鼻气管炎病毒、牛病毒性腹泻病毒和牛支原体引物的三个浓度,先后设计8组引物浓度配比组合(表3),在保证扩增效率的基础上,考虑试剂成本后筛选出引物浓度的最佳配比组合。使用同样的方法筛选出探针浓度的最佳配比组合。引物和探针浓度的最佳配比组合确定后,对退火温度(52~62℃)(表5)进行进一步的优化,最终确定三重荧光PCR的反应体系和反应程序。由表3~表5可以得出,牛传染性鼻气管炎病毒、牛病毒性腹泻病毒和牛支原体的最佳引物组合为IBRV+BVDV+Mb=0.3μM+0.4μM+0.3μM,最佳探针组合为IBRV+BVDV+Mb=0.15μM+0.2μM+0.15μM,最佳退火温度为52℃,因此,三重荧光PCR的最终反应体系见表6,反应程序具体为:反转录42℃5min;预变性94℃30s;变性94℃5s,退火55℃30s,40个循环数。使用最佳反应体系和反应程序扩增阳性参考品和阴性参考品(无核酶水),其扩增曲线如图1所示,阳性参考品有扩增曲线,而阴性参考品无扩增曲线,表明该反应体系和反应程序对牛传染性鼻气管炎病毒、牛病毒性腹泻病毒和牛支原体的混合样品均有良好的扩增效果。
[0081]表3引物浓度组合优化结果
[0082]
[0083]表4探针浓度组合优化结果
[0084]
[0085]表5退火温度优化结果
[0086]
[0087]
[0088]表6三重荧光PCR检测反应体系
[0089]
PUM
 Login to View More
Login to View More Abstract
Description
Claims
Application Information
 Login to View More
Login to View More